
- Автор Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:38.
- Акыркы өзгөртүү 2025-01-22 17:04.
ВИДЕО
Анда атомдук массалардын көйгөйлөрүн кантип чечесиз?
үчүн эсептөө the атомдук масса элементтин бир атомунун, кошуу масса протондордун жана нейтрондордун. Мисал: табыңыз атомдук масса 7 нейтрон бар көмүртек изотопунун. Көмүртектин бар экенин мезгилдик таблицадан көрө аласыз атомдук саны 6, бул анын протондорунун саны.
Мындан тышкары, атомдук массалык саны деген эмне? The массалык саны (А символу, немисче Atomgewicht сөзүнөн [ атомдук салмагы]) деп да аталат атомдук масса саны же нуклон саны , жалпы болуп саналат саны протондор менен нейтрондордон (бирге нуклондор деп аталат). атомдук ядро. The массалык саны химиялык элементтин ар бир изотопу үчүн ар кандай болот.
Ошондой эле билүү керек, атомдук массанын формуласы кандай?
Орточо атомдук масса = f1М1 + f2М2 +… + f М мында f - изотоптун табигый көптүгүн билдирген бөлүк, ал эми M - бул масса изотоптун саны (салмагы). Орточо атомдук масса элементти мезгилдик таблицада, адатта, элементардык символдун астында тапса болот.
Химияда орточо атомдук масса деген эмне?
The орточо атомдук масса элементтин суммасы болуп саналат массалар анын изотопторунун ар бири табигый көптүгүнө көбөйтүлөт (пайыз менен байланышкан ондук сан атомдор берилген изотоптун элементи).
Сунушталууда:
Теңдемелер системасынын сөз маселелерин кантип чыгарасыз?

Теңдеме сөз маселелери системасын чечүү үчүн биз адегенде өзгөрмөлөрдү аныктайбыз, андан кийин сөз маселелеринен теңдемелерди чыгарабыз. Андан кийин биз системаны графикалык, жок кылуу же алмаштыруу ыкмаларын колдонуу менен чече алабыз
Стронцийдин орточо атомдук массасын кантип эсептейсиз?

Ошентип, биз изотоптордун ар биринин салмактуу массасын алып, аларды кошуп эсептейбиз. Ошентип, биринчи масса үчүн 84 (аму - атомдук масса бирдиктери) = 0,042 амудан 0,50% көбөйтүп, аны 86 аму = 8,51 амудан 9,9% кошобуз ж.б.у.с
Бордун атомдук массасын кантип эсептейсиз?
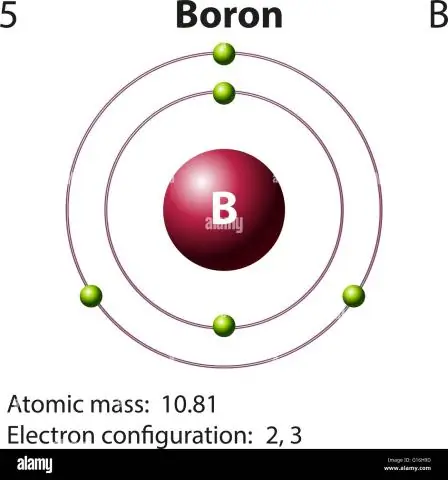
Бор үчүн бул теңдеме мындай болот: 5 протон + 5 нейтрон = 10 атомдук масса бирдиги (AMU) же көбүнчө кездешкен бор изотопу үчүн (болжол менен 5 протон + 6 нейтрон = 11 AMU)
Титрлөө маселелерин кантип эсептейсиз?

Титрлөө маселеси Этап-этабы менен чечүү 1-кадам: [OH-] аныктагыла NaOH ар бир молунда бир моль OH- болот. 2-кадам: OH моль санын аныктаңыз- Молярдуулук = моль/көлөмдүн саны. 3-кадам: H+ моль санын аныктоо 4-кадам: HCl концентрациясын аныктоо
Эмне үчүн мезгилдик таблица атомдук масса менен эмес, атомдук саны боюнча түзүлгөн?

Эмне үчүн Мезгилдик таблица атомдук масса менен эмес, атомдук саны боюнча жайгаштырылган? Атомдук номер – ар бир элементтин атомдорунун ядросундагы протондордун саны. Бул сан ар бир элемент үчүн уникалдуу. Атомдук масса протондор менен нейтрондордун бириккен саны менен аныкталат
