
Мазмуну:
- Автор Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:38.
- Акыркы өзгөртүү 2025-01-22 17:04.
Льюисди тарт жеке атомдордун символдору молекула . Атомдорду ар бир атомдун айланасына сегиз электрон (же H үчүн эки электрон) жайгаштыргандай кылып бириктириңиз. суутек ) мүмкүн болгон жерде. Бөлүштүрүлгөн электрондордун ар бир жуп а коваленттик байланыш сызыкча менен көрсөтүлүшү мүмкүн.
Буга байланыштуу, кошулма үчүн Льюис структурасын кантип тартасыз?
Бул нускамалар молекулалар үчүн Льюис структураларын тартуу үчүн Келтердин стратегиясын баяндайт
- 1-кадам: Валенттик электрондордун жалпы санын табыңыз.
- 2-кадам: Атомдорду "бактылуу" кылуу үчүн керектүү электрондордун санын табыңыз
- 3-кадам: Молекуладагы байланыштардын санын аныктоо.
- 4-кадам: Борбордук атомду тандаңыз.
Ошондой эле билесизби, сиз облигация тартибин кантип табасыз? Молекулада экиден ашык атом болсо, байланыш тартибин аныктоо үчүн төмөнкү кадамдарды аткарыңыз:
- Льюис структурасын тартыңыз.
- Облигациялардын жалпы санын эсептеңиз.
- Жеке атомдордун ортосундагы байланыш топторунун санын эсептегиле.
- Атомдордун ортосундагы байланыштардын санын молекуладагы байланыш топторунун жалпы санына бөлүңүз.
Ошо сыяктуу эле, коваленттик байланыштар кандай түзүлүштү түзүшөт?
Коваленттик байланыштар электрон тыгыздыгын бөлүшкөн эки атомду, адатта металл эместерди камтыйт форма күчтүү байланыш өз ара аракеттенүү. Коваленттик байланыштар бир, эки жана үчтүк камтыйт облигациялар жана тиешелүүлүгүнө жараша 2, 4 же 6 электрон бөлүшүлгөн сигма жана пи байланыштын өз ара аракеттешүүсүнөн турат.
bf3 түзүлүшү кандай?
молекуласынын геометриясы BF3 'Trigonal Planar. ' Химия шилтемеси менен, 'Trigonal Planar' ортосунда бир атомдун тегерегинде үч атом бар модель. Бул бардыгы бир тегиздиктеги перифериялык атомдор сыяктуу, анткени алардын үчөө тең ар биринин 120° байланыш бурчтары менен окшош, бул аларды тең жактуу үч бурчтук кылат.
Сунушталууда:
Өсүмдүк клеткасын кантип тартасыз?

ВИДЕО Анан кантип этап-этабы менен бир өсүмдүк тартуу керек? Кадамдар Керектүү нерсени чогулт. Негизги түзүлүштү тик бурчтуктан сызык менен баштаңыз. Төрт бурчтуктун астына үстөл жаса (кийин казанга айланат). Тик бурчтуктан чыккан сызыкка жалбырактарды кошуңуз.
Молекулярдык геометрияны кантип тартасыз?

Молекуланын формасын табуу үчүн колдонулган кадамдар Льюис структурасын түзүшөт. Электрондук топтордун санын санап, аларды электрон топторунун байланыш жуптары же электрондордун жалгыз жуптары катары аныктаңыз. Электрондук топтун геометриясын атаңыз. Борбордун айланасындагы башка атомдук ядролордун абалын карап, молекула геометриясын аныктайт
Ылдамдык менен убакыт графигин кантип тартасыз?
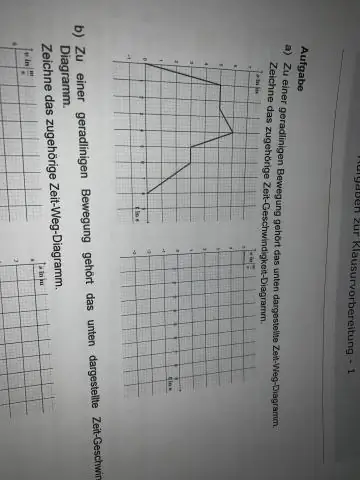
График кагазына бир чекиттен башталган жана бири-бирине перпендикуляр болгон эки түз сызыкты тарткыла. Бул x-y огу. X огу горизонталдык сызык жана у огу вертикалдуу сызык. Таблицадан убакыттын маанилерин оңой графикте алуу үчүн x огунда бирдей аралыктагы тиешелүү убакыт интервалдарын белгилеңиз
Льюис кислотасы Льюис негизи менен аракеттенгенде кандай байланыш түзүлөт?

Координаттык коваленттик байланыш
Кайсы аминокислота белоктун үчүнчү структурасын турукташтырат?

Бул карым-катнаштар алыскы аминокислоталарды жакындатуу үчүн белок чынжырына бүктөлүү аркылуу мүмкүн болот. 2. Үчүнчү түзүлүш дисульфиддик байланыш, иондук өз ара аракеттенүү, суутек байланышы, металлдык байланыш жана гидрофобдук өз ара аракеттенүү аркылуу турукташтырылган
